73歲男性,胸痛持續。需要導管介入嗎?
覺得這個Case非常有趣,也可以從中學到不少。特地把這個Case從眾多想寫的案例中,往前拉。
73歲男性,半夜來就診。因為胸痛厲害,所以當班急診醫師也做了Chest CTA去排除主動脈剝離。
早上我接班後,我自己的習慣會去把交班主述胸痛的病患,再去看一眼,前一班所做的心電圖。病患一開始的TnI為0.26 mg/mL,已經是>99th percentile of URL。預計之後會在抽第二次心臟酵素。
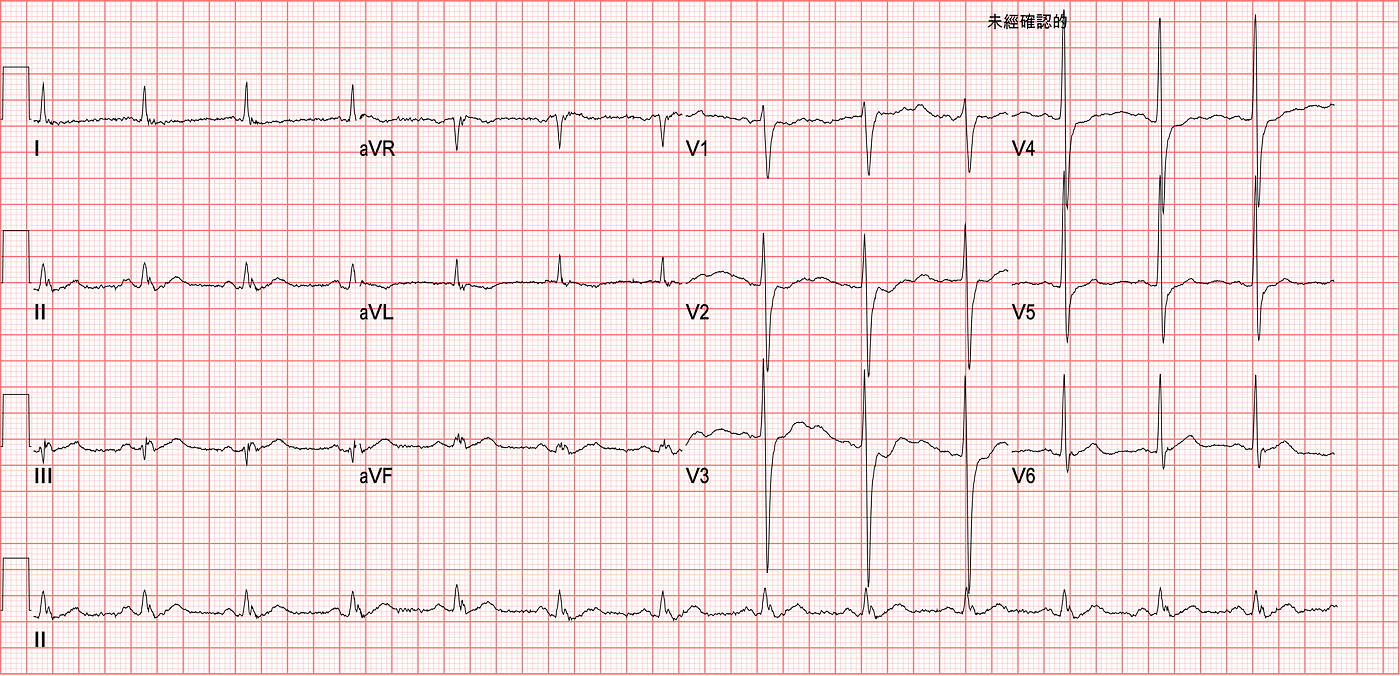
Initial ECG如上圖,我看完後,就直接去看病患,看看目前病患的胸痛狀況目前如何?
各位有看到什麼嗎?
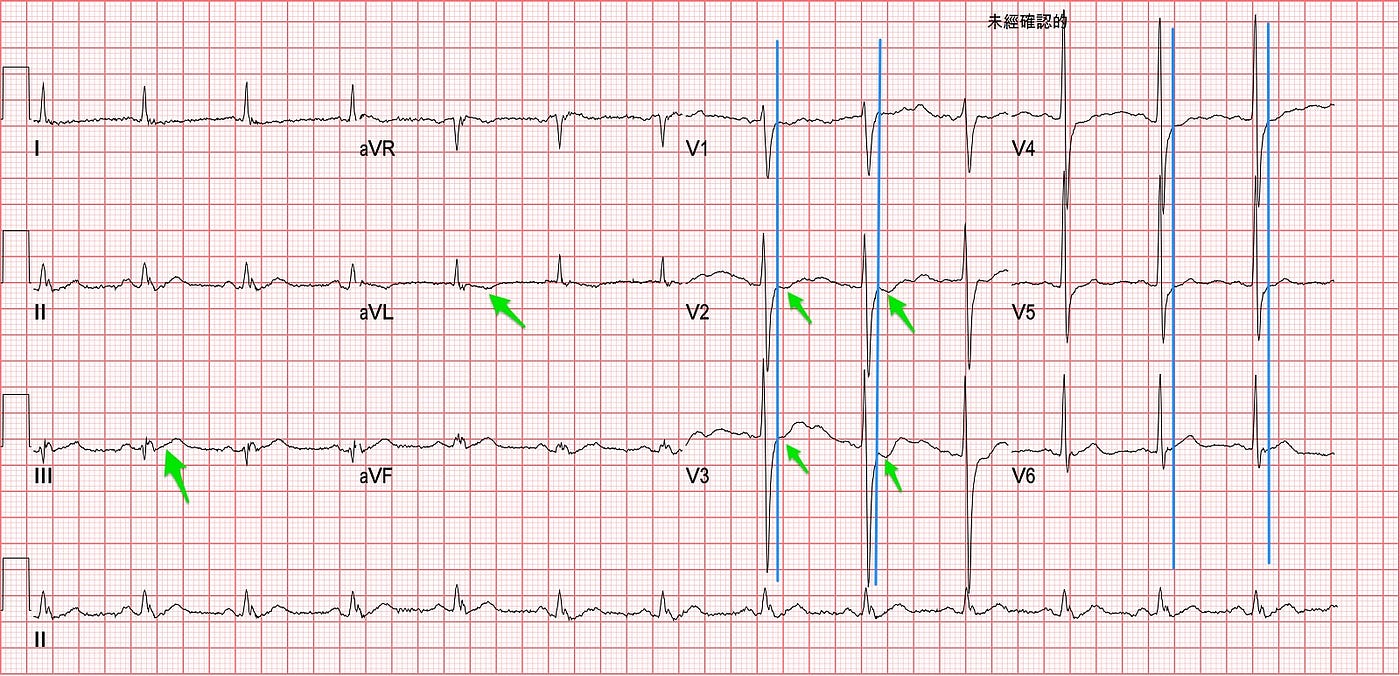
垂直藍線是畫在J point。J point是用來評估是否有STE or STD的點。J point是QRS的結尾到ST segment的開頭。若是在Baseline以上就是STE,baseline以下就是STD。
我們要運用STEMI criteria就是要看根據J point的位置來判斷是否有STE,才能夠診斷STEMI。 在最近的2018年第四版的Universal Definition of Myocardial Infarction裡面就有清楚講明什麼是AMI。什麼可以叫做STEMI。

AMI就是出現Myocardial injury的證據(Biomarker上升)+ Myocardial ischemia證據(症狀 or ECG or 影像出問題)。(Fig.2)
而要診斷STEMI,則必須符合STEMI criteria。(Fig.3)

必須要再三強調,V2/V3的STE與其他lead定義不一樣。看V2/V3要根據性別/年齡合併一起看。
舉例來說,男性<40 y/o在V2/V3要≧2.5 mm才是有意義的高。其他以此類推。
這延伸了幾個有趣的狀況:
- 這也代表著,隨便抓一個人來作12 lead ECG,很有可能會在V2/V3都看到有STE,只是有沒有意義的高,就需要根據上述的criteria了。
- 如果沒有看到STE在V2/V3(比如isoelectric baseline or minimal STD),那麼就需要考慮是不是有什麼力量往下拉了。對~~~Post.OMI
- 承上面,怎樣程度的minimal STD都要考慮Post.OMI呢?
在這篇Smith ECG Blog有提到¹,在V2 or V3有任何程度的STD,都必須考慮posterior OMI,直到證明不是為止。特別是downsloping STD(符合前述,即使STD<0.5~1 mm都要特別小心)
Ken Grauer與Smith大師,多次強調V2 or V3的ECG morphology。除了前述的任何程度的STD。如果出現downsloping STD or Shelf-like STD都要小心有Post.OMI.
在這一篇之前寫的文章中,我有更詳盡的論述,要如何診斷Post.OMI²。簡短說一下:STDmaxV1–4(+) →直指Post.wall MI,直到排除為止(翻成白話文就是在precordial leads出現STD,且STD的最大值是出現在V1-V4其中一個lead,就要考慮後壁梗塞)。
Back to Case
在Fig.1當時我看到在V2/V3似乎有出現downsloping STD,不過Baseline並不是很穩,但是如果光看V2,三個beat似乎都有。
另外aVL出現TWI且III/aVF的ST segment是straight的,這種ST segment morphology,Amal mattu在教學時常常會說這種morphology叫做Checkmark sign(打勾)。一般正常的STE是Concave(凹向上),當出現下列狀況就必須考慮ischemic pattern STE morphology。(Fig.5-A)
另外在Lead II/III的T wave相對於前面的QRS,算是HATW。

當時交班後,因為看了這張ECG,認為這些lead都出現了ischemic ECG morphology,所以心中高度懷疑病患有OMI,但是因為ECG沒有符合任何STEMI criteria,所以很容易就會被missed掉。
到了病患Bedside,病患表示仍胸痛。於是立馬再做了一張ECG(Fig.6)
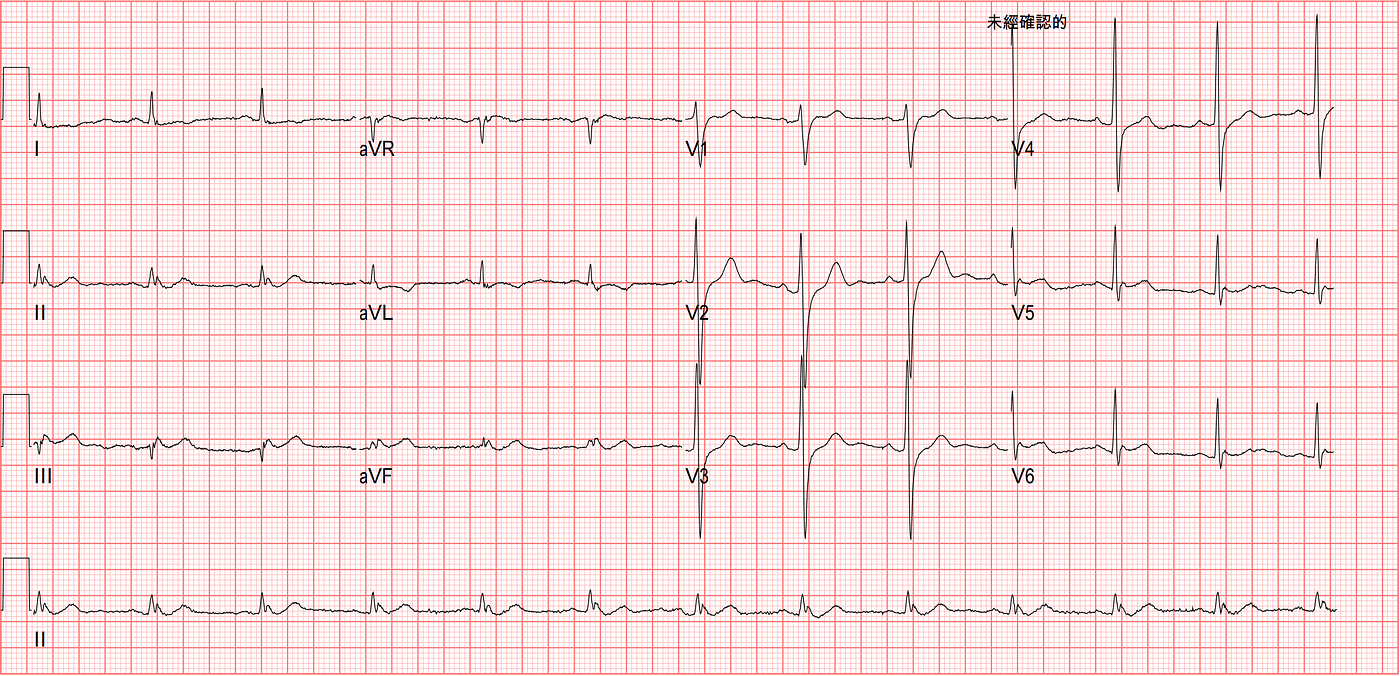
Fig.6是病患第二張ECG,大概是到院後的三小時。V2 or V3已經沒有看到downsloping STD pattern。但是Lead III/aVF其ST segment仍是straight與T wave仍是HATW。aVL的T wave為TWI。這張ECG還是沒有達到STEMI criteria的標準,但確確實實是OMI。
為了能有更多的myocardial ischemia證據,再度拿出Lumify。
PSAX的papillary muscle view可以看到lateral wall和inferior wall動得都不是很好(RWMA+)。(Fig.7)
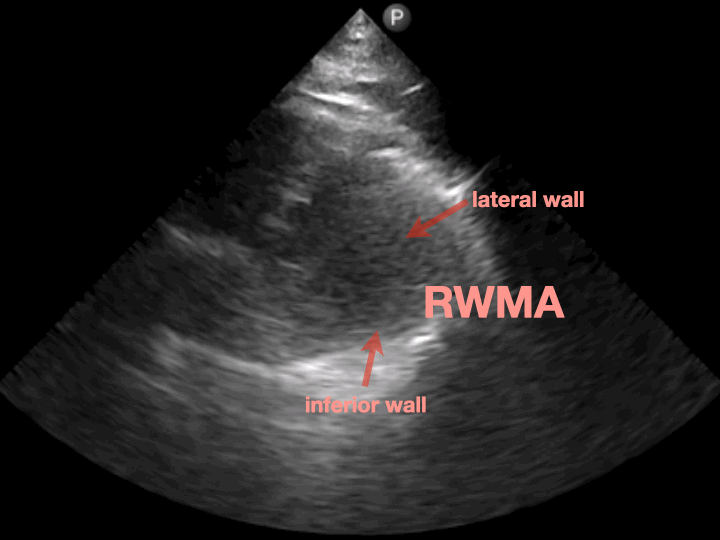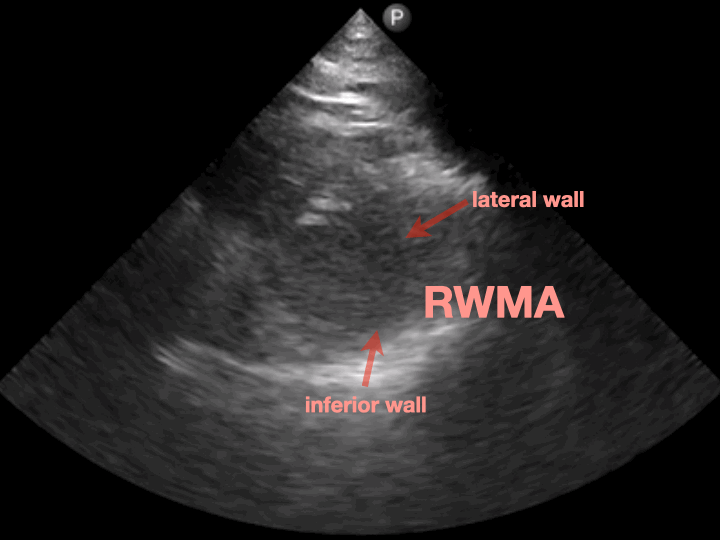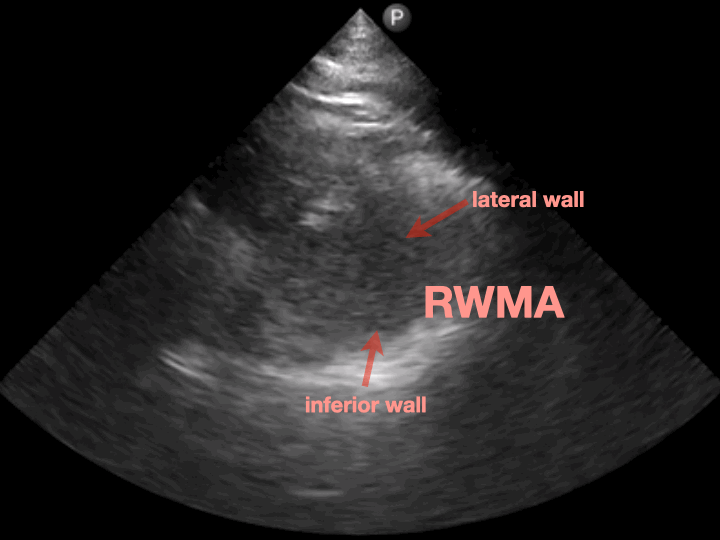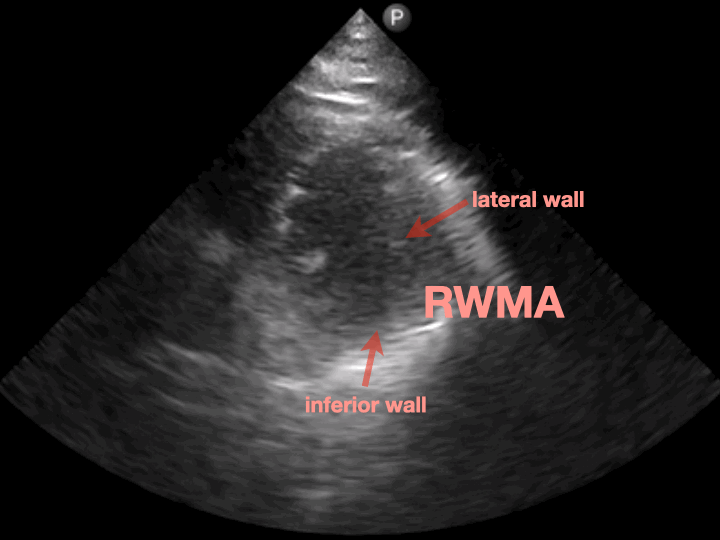
這個echo finding符合ECG缺血的區域。
另外病患也有在前一班做了Chest CTA去排除主動脈剝離。
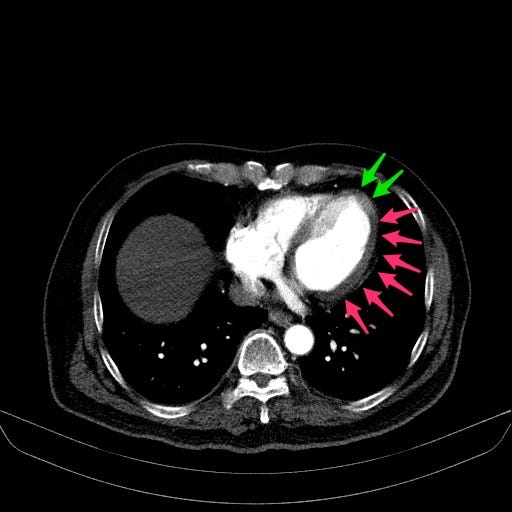
Fig.8可以看到在Chest CTA下lateral wall of LV,比較偏向外側區塊有hypoperfusion(這也就是下面會說到的myocardial perfusion defect)的狀況(紅色偏暗區塊)。這也符合ECG與echo的findings。
這邊我們需要提出一個問題,那就是這個在non-ECG-gated contrast-enhanced CT下看到的hypoperfusion,有沒有其他可能性?可不可信?
各位有興趣可以參考這一篇文章³。我這邊總結幾項這篇的論點:
- Cardiac CT(coronary CTA)可以幫助我們評估coronary artery stenosis,此外也可以評估myocardial perfusion defect(MPD)(也就是像Fig.8一樣出現LV hypodense lesion)。但是Coronary CTA需要ECG gating,此外也需要高階多切的MDCT。
- 然而有不少最近的研究描述(請見Fig.9),ACS可以在一般routine所做的non-ECG-gated contrast-enhanced CT藉由測到myocardial perfusion defect而做出診斷。
- 雖然使用ECG-gated MDCT影像對各種心臟疾病的成像效果較佳,但通常在non-ECG-gated contrast-enhanced CT也能提供足夠的信息,以識別一些意外發現的心臟異常,例如可能與患者主訴症狀有關的myocardial perfusion defect(MPD)。
- Cardiac motion artifacts仍然是影響non-ECG-gated contrast-enhanced CT診斷ACS的最大因子
- 出現myocardial perfusion defect但是卻沒有myocardial ischemia,主要是因為cardiac motion artifacts導致(false-positive →假陽性),這種狀況的frequency只有15–20%,並不高。
- 另外在ACS個案中,因為AMI降低了局部myocardial wall motion,也會促使cardiac motion artifacts的降低,並且讓心肌邊界更清楚(這是壞事也是好事XD)
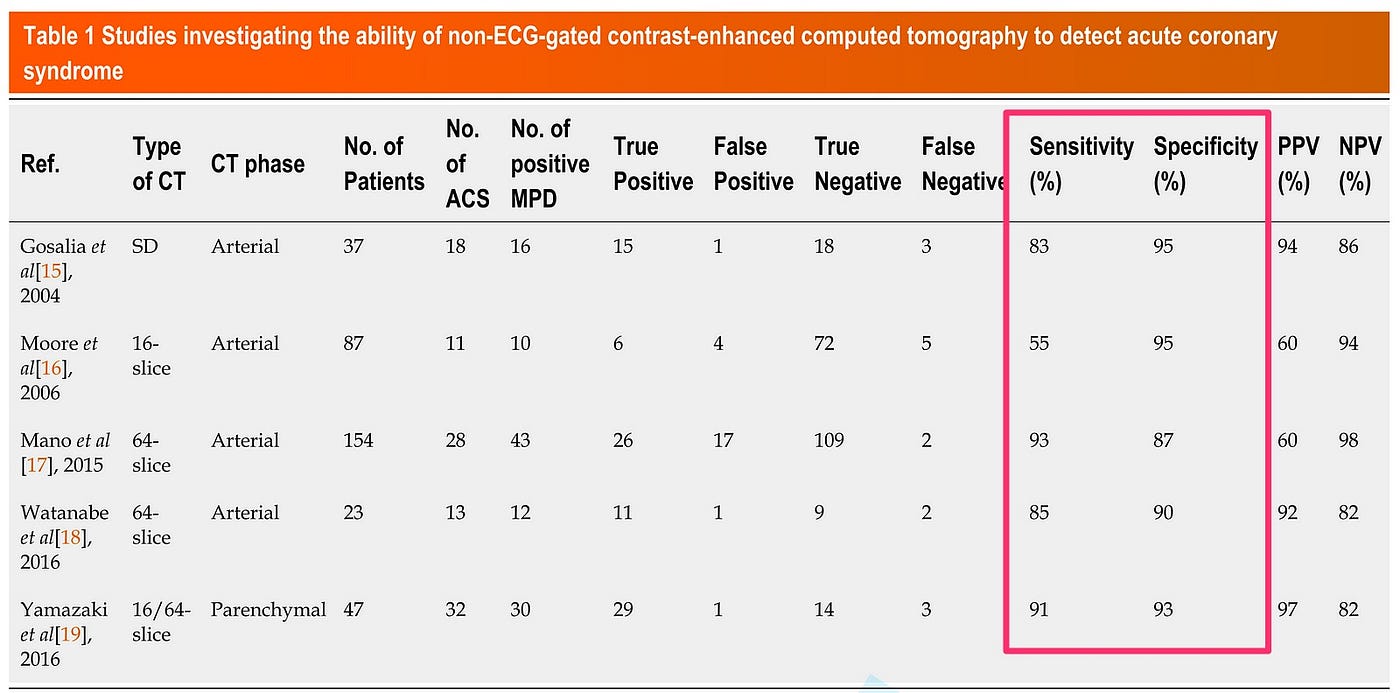
根據Fig.9,在non-gated-ECG contrast-enahnced CT如果看到myocardial perfusion defect(MPD)對於診斷ACS有不錯的sensitivity與specificity。
總之這一篇表示出,為了避免沒有治療到此危及性命的狀況(如ACS),臨床醫師應該要警覺了解,即使在一般non-ECG-gated contrast-enhanced CT,如果有ACS也會常見myocardial perfusion defect。
Back to Case
當時對於病患有OMI的證據越來越多:
- ECG在inf.leads有HATW、straight ST segment(Checkmark sign+),initial ECG出現downsloping STD in V2/V3
- Echo顯示有RWMA在inf./lateral wall
- Non-ECG-gated contrast enhanced CT出現myocardial perfusion defect
且這三者符合特定的冠狀動脈支配區域。
另外病患在給了內科療法,仍持續胸痛。根據ESC 2020 NSTEMI guideline,屬於Very high risk feature病患⁴。
如果我們沒辦法辨識出這個病患有OMI。依照目前STEMI/NSTEMI paradigm的分類。這位病患理應被分類到NSTEMI這一類中(TnI⬆︎加上myocardial ischemia證據)。剛剛說過,refractory ischemic chest pain算是very high risk feature,所以這位病患應該要在2小時內安排到PCI,看血管有沒有阻塞(見Fig.10)。
Fig.10應該是我的心電圖Blog,出現最多次的一張圖吧XD
要注意Fig.10的Very high risk feature,裡面幾乎沒有提到心電圖要變成怎樣,才要緊急做到PCI(唯一例外有講到是aVR STE+ ≧ 6個leads出現STD)。也就是病患出現反覆胸痛,治療沒反應。就應該Call CV man評估是否心導管。而不是猛作ECG,看會不會變成STE。
當然如果serial ECG出現STE很好,因為CV man肯定要買帳殺進去。
但是….也就是這個但是…..
上個月Smith ECG有一篇文章⁵裡面比較了STEMI/NSTEMI paradigm與OMI/NOMI paradigm的差別,裡面有一點講到serial ECG。
我重點條列一下:(這不是ChatGPT寫的啦)
- 在STEMI/NSTEMI paradigm,病患有缺血症狀並且ECG並不符合STEMI criteria,此時會進行serial F/U ECG➡但是STEMI criteria對於ACO的sensitivity不高(意思是病患血管有阻塞,但是會以STE表現出來的狀況不多,有更多是以非STE的ECG pattern來表現)
- STEMI(-)/OMI(+)的患者可能會多次接受心電圖檢查,這些檢查反覆顯示為 OMI的診斷(就像我這個Case),但卻反覆未達到STEMI criteria➡通常這些serial F/U ECG不會演變成符合STEMI criteria,總是在最佳可以進行intervention的時機點過了才會有所變化(靠!!!好奸詐XD)
- Serial ECG來尋找 STEMI criteria有可能會繼續錯失STEMI(-)/OMI(+)導致Delayed PCI
所以Serial F/U ECG企圖找尋STE的出現,有可能會讓這個病患delayed PCI,因為通常STEMI(-)/OMI(+),有可能不會演變成STEMI(+)/OMI(+)。
所以只要符合NSTEMI + Very high risk feature →請Call CV man
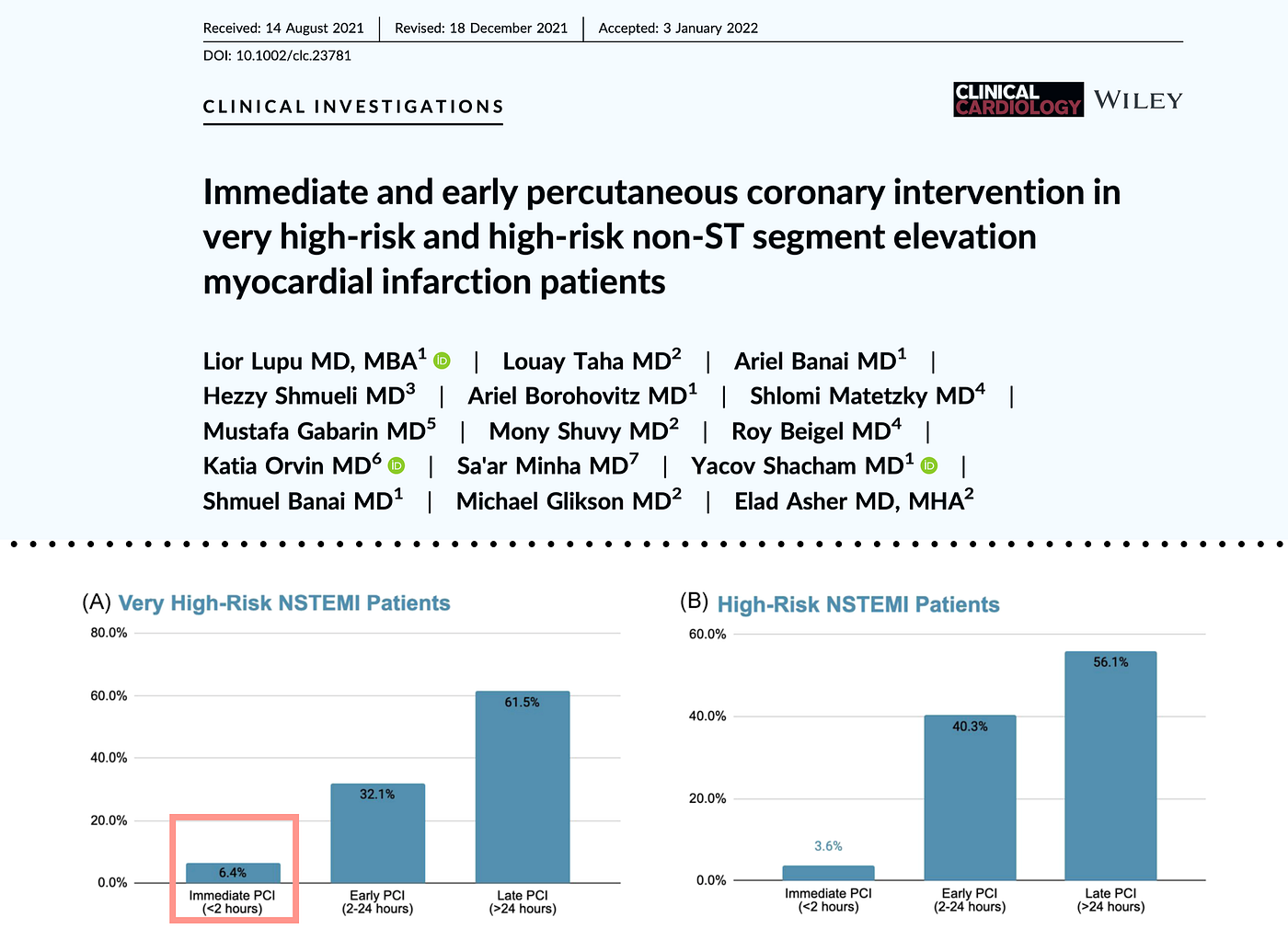
雖然我們知道NSTEMI符合Very high risk feature的病患在<2小時被抓去作PCI的比例很低。這全世界都如此(Fig.11)。
但是不要氣餒,總是會有成功能夠幫助到病患的時候
回到此個案~~
所以我把我的擔憂,親自打電話告知CV man。CV man,同意我的說法,並且願意立刻幫病患作心導管。
我在電子病歷上打上最後的文字,緊接著病患就上去作導管了。
CAG報告: LCx total occlusion➡CAD with TVD s/p CAG, with LAD 50–60% occlusion, RCA: CTO, LCX total occlusion, DES*1 over LCX
文章重點:
- 如何診斷Classic STEMI(V2/V3定義不同)
- AMI定義(Fig.1)
- V2/V3如果是minimal STD or isoelectric basline有意義嗎?
- Ischemic pattern的STD(downsloping/Shelf-like STD)
- 在non-ECG-gated contrast-enhanced CT看到Myocardial perfusion defect(MPD),可信嗎?
- STEMI(-)/OMI(+),通常不會演變成符合STEMI criteria的STEMI(+)/OMI(+)
- 熟知NSTEMI有哪些狀況算是very high risk feature
- 如果心中擔憂病患有OMI,但是卻沒有符合STEMI criteria的ECG出現,尋找更多OMI的證據(Serial F/U ECG、TnI、Echo)。親自打電話告知CV man,我們的想法如何,或許可以幫助病患提早做到PCI,減少病患心臟細胞的失去。
參考資料:
- Dr. Smith’s ECG Blog: Any ST depression in V2 and V3 is posterior OMI until proven otherwise, especially if downsloping — link
- 這是STEMI,你相信嗎?. 來看看昨天夜班上班的一位個案。50歲男性,本來從事捕鰻苗的工作。 | by Tsao Jian-hsiung | Medium — link
- Yoshihara, S. (2022). Acute coronary syndrome on non-electrocardiogram-gated contrast-enhanced computed tomography. World Journal of Radiology, 14(2), 30–46. https://doi.org/10.4329/wjr.v14.i2.30
- Collet, J.-P., Thiele, H., Barbato, E., Barthélémy, O., Bauersachs, J., Bhatt, D. L., Dendale, P., Dorobantu, M., Edvardsen, T., Folliguet, T., Gale, C. P., Gilard, M., Jobs, A., Jüni, P., Lambrinou, E., Lewis, B. S., Mehilli, J., Meliga, E., Merkely, B., … ESC Scientific Document Group. (2021). 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. European Heart Journal, 42(14), 1289–1367. https://doi.org/10.1093/eurheartj/ehaa575
- Dr. Smith’s ECG Blog: 50 year old with acute chest pain, with ‘normal’ ECG and falling troponin — link
